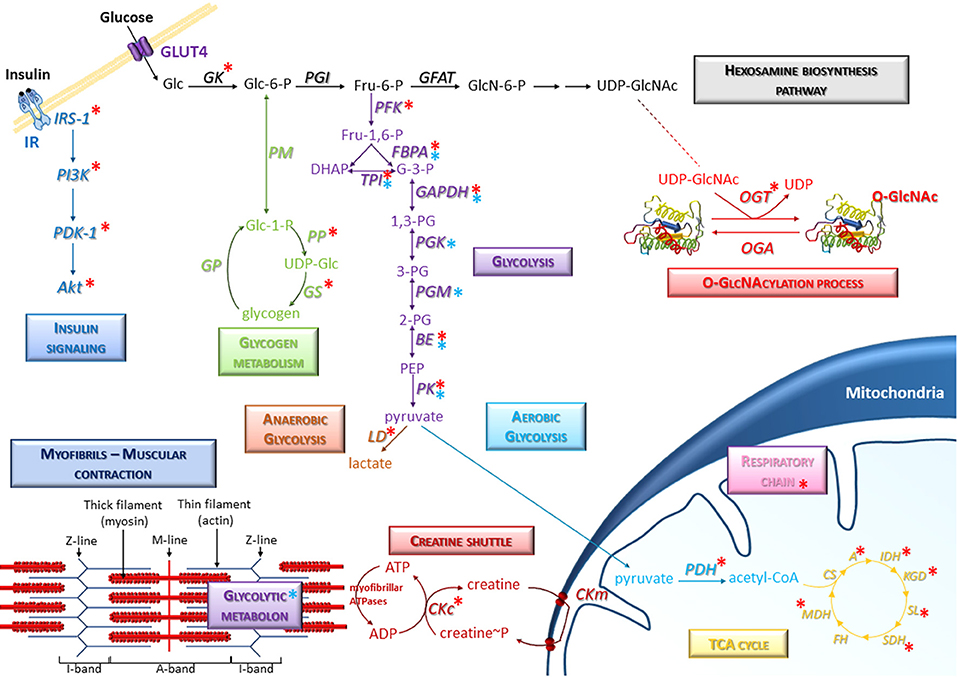
Edustava kaava luustolihaksessa tapahtuvasta heksosaminibiosynteesitiestä, jossa muodostuu O-GlcNAc ja tapahtuu posttranslationaalinen lisääminen solussa oleviin proteiineihin transferaasilla OGT / tai tämän ryhmän poisto OGA hydrolaasilla). kuvan oiekassa yläkulmassa.
kuvassa esitetään myös miten insuliini signaloituminen tapahtuu IR insuliinireseptoriteitse, jolloin aktivoituu signaalitie IRS-1- PI3K-PDK1-Akt.
Glukoosin tulo soluun tapahtuu GLUT4-proteiinin avulla ja sitten kinaasi fosforyloi sen Glukoosi-6 fosfaatiksi. Siitä voi osa mennä glykogeeniaineenvaihduntaan, jolloin sen täytyy ensin muuttau Glukoosi-1-fosfaatiksi ja aktivoitua UTP-energialla. UDP-glukoosiksi, josta voi syntetisoida lihasglykogeeniä.
Osa soluun tulleesta glukoosista jatkaa muuttumalla fruktoosiksi Fru-6-P ja siten fruktoosi-bifosfaatiksi ja menee glykolyysiteihen. Palorypälehappovaiheesta voi osa mennä anaaerobiseen glykolyysiin tarvittaessa ja siitä tulee vähän ATP:tä ja lopulta maitohappoa. Aerobinen glykolyysi tuottaa paljon ATP:tä mitokondriasta. Lihaksessa ATP-energiaa voidaan slussata lihakseen kreatiniinislussin avulla . Myosiinissa on omia ATPaaseja. Entsyymien nimiå alla. Ne kuuluvat kuvan selitykseen.
- Representative scheme of the presence of O-GlcNAcylation on glucose metabolism in skeletal muscle. Several signaling and metabolic pathways are indicated, in particular the hexosamine biosynthesis pathway, glycolysis (anaerobic and aerobic glycolysis), glycogen metabolism, insulin signaling, and TCA cycle. Specific molecular components of skeletal muscle such as myofibrils and creatine shuttle are also represented. Red asterisks correspond to O-GlcNAcylated proteins; blue asterisks correspond to enzymes including in protein-protein complexes (such as the glycolytic metabolon) which could be potentially modulated consecutively to O-GlcNAcylation changes in skeletal muscle cells. A, Aconitase; BE, Beta-enolase; CKc, Creatine kinase cytoplasmic; CKm, Creatine kinase mitochondrial; CS, Citrate synthase; FBPA, Fructose-bisphosphate aldolase; FH, Fumarate hydratase; GAPDH, Glyceraldehyde-3-phosphate dehydrogenase; GFAT, Glutamine,fructose-6-phosphate aminotransferase; GK, Glucokinase; GP, Glycogen phosphorylase; GS, Glycogen synthase; IDH, Isocitrate dehydrogenase; KGD, Ketoglutarate dehydrogenase; LD, Lactate dehydrogenase; MDH, Malate dehydrogenase; OGA, O-GlcNAcase; OGT, O-GlcNAc transferase; PDH, Pyruvate Dehydrogenase; PFK, Phosphofructokinase; PGI, Phosphoglucose isomerase; PGK, Phosphoglycerate kinase; PGM, Phosphoglycerate mutase; PK, Pyruvate kinase; PM, phosphoglucomutase; PP, UDP-glucose pyrophosphorylase; SDH, Succinate Dehydrogenase; SL, Succinyl-CoA ligase; TPI, Triose-phosphate isomerase.
LUUSTOLIHAS ( tahdonalainen lihaksisto) käsittää 40 % koko kehonpainosta. Lihaksen päätehtävä on konvertoida kemiallinen energia mekaaniseksi energiaksi, mikä takaa voiman generoitumista liikkeisiin ja lokomotioon ja pitää yllä asentoa. Ratkaisevasta energiariippuvuudesta vastaa lihaksisto, joka on keskeinen koko kehon aminohappojen ja hiilihdydraattien varasto. Juuri näistä ravintoaineista muun muuassa riippuu posttranslationaalinen modifikaatio N-asetyyliglukosaminin (GlucNAc) liittäminen -O- asemaan entsyymeissä (O-GlucNAc-) Siinä siirretään tai tarvitatessa irrotetaan näitä ainutlaatuisia monosakkarideja ( N-asetyyli-D-glukosamineja) aminohappojen seriinin tai treoniini OH-ryhmään nukleosytoplasmisessa tai mitokondriaalisessa proteiinissa. Prosessi on dynaaminen: ja tapahtuu entsyymien O-GlcNAc- transferaasin (OGT) tai vastaavasti O-GlcNAc-glykosidihydrolaasin (OGA) katalysoimina reaktioina. Tämä heksosamini on rakenteellinen sokeri ja sillä on paljon merkitystä typpipitoisena aminosokerina solujen pintarakenteissa ja proteiinien ikää pidentävissä tekijöissä.
OGT = O-linkkiytynyt N-asetyyliglukosaminyylitransferaasi
OGA , 3-O-(N-asetyyli-D-glukosaminyyli) L-seriini/treoniini N-asetyyliglukosaminyylihydrolaasi
tai lyhemmin sanottuna O-GlcNAcaasi
(Selitys:
Glukosamini on hiilihydraattiaineenvaihdunnasta peräisin oleva sokeri glukoosi, jossa on aminohapon glutamiinihapon amidityppi (N) liitetty sokeriin.
Tämä glukosamini on sitten asetyloitu, saanut Ac- ryhmänsä.
Nyt se on GlcNAc
Sitten se on liitetty proteiinissa olevan aminohapon OH- ryhmään sen O -molekyyliin, joten saadaan O-GlcNAc . Nyt on sokeriaineenvaihdunnasta kehittynyt rakenteellinen molekyyli, jonka avulla saadaan erilaisia glykokonjugaatteja proteiineille. Ihmiskehon rakenneaminohapoista seriinillä ja treoniinilla on OH- ryhmät rakenteessa. Seriini ja treoniini (s ja t) kuuluvat niihin aminohappoihin joita ihmisen genomi koodaa).
Abstract
- Skeletal muscle represents around 40% of whole body mass. The principal function of skeletal muscle is the conversion of chemical energy toward mechanic energy to ensure the development of force, provide movement and locomotion, and maintain posture. This crucial energy dependence is maintained by the faculty of the skeletal muscle for being a central place as a "reservoir" of amino acids and carbohydrates in the whole body. A fundamental post-translational modification, named O-GlcNAcylation, depends, inter alia, on these nutrients; it consists to the transfer or the removal of a unique monosaccharide (N-acetyl-D-glucosamine) to a serine or threonine hydroxyl group of nucleocytoplasmic and mitochondrial proteins in a dynamic process by the O-GlcNAc Transferase (OGT) and the O-GlcNAcase (OGA), respectively.
Ensimmäiset saadut oivallukset antoivat viitettä jonkin verran erilaisiin OGT/OGA ilmentymisiin ja /tai aktiivisuuksiin ja erilaisiin solustressivasteisiin (ROS, reaktiivisiin happilajeihin ja/tai HSP-proteiineihin).
Vankkaa tietoa tuli siitä, että nämä O-GluNAc-muutokset voisivat johtaa
(1) hiilihydraattiaineenvaihdunnan erilaisiin moduloitumisiin, koska tiedetään suurimman osan entsyymeistä saavan posttranslationaalisen O-GlcNAc- lisukkeen ja
(2) proteiinisynteesi/proteiininhajoitustasapainon erilaiseen modulaatioon, koska O-GlcNAc -päätteen saaminen säätelee luustolihaksessa muutamia avainasemassa olevia signaaliteitä kuten Akt/GSK3beeta, Akt/mTOR, myogeniini/atrogiini-1, myogeniini/Mef2D, Mrf4 ja PGC-1alfa.
- O-GlcNAcylation has been shown to be strongly involved in crucial intracellular mechanisms through the modulation of signaling pathways, gene expression, or cytoskeletal functions in various organs and tissues, such as the brain, liver, kidney or pancreas, and linked to the etiology of associated diseases. In recent years, several studies were also focused on the role of O-GlcNAcylation in the physiology and the physiopathology of skeletal muscle. These studies were mostly interested in O-GlcNAcylation during muscle exercise or muscle-wasting conditions. Major findings pointed out a different "O-GlcNAc signature" depending on muscle type metabolism at resting, wasting and exercise conditions, as well as depending on acute or long-term exhausting exercise protocol. First insights showed some differential OGT/OGA expression and/or activity associated with some differential stress cellular responses through Reactive Oxygen Species and/or Heat-Shock Proteins. Robust data displayed that these O-GlcNAc changes could lead to (i) a differential modulation of the carbohydrates metabolism, since the majority of enzymes are known to be O-GlcNAcylated, and to (ii) a differential modulation of the protein synthesis/degradation balance since O-GlcNAcylation regulates some key signaling pathways such as Akt/GSK3β, Akt/mTOR, Myogenin/Atrogin-1, Myogenin/Mef2D, Mrf4 and PGC-1α in the skeletal muscle.
- Finally, such involvement of O-GlcNAcylation in some metabolic processes of the skeletal muscle might be linked to some associated diseases such as type 2 diabetes or neuromuscular diseases showing a critical increase of the global O-GlcNAcylation level.
Inga kommentarer:
Skicka en kommentar