NOTCH-proteiinit ovat transmembraanisia ja niitä aktivoi erilaiset ligandit. Aktivoinnista seuraa, että proteiinin solunsisäinen domeeni pilkkoutuu ja translokoituu solun tumaan, jossa se aiheuttaa transkriptionaalista aktiivisuutta.
Löysin hyvän videon Notch signaloinnin periaatteesta:
https://www.youtube.com/watch?v=kFXrJLxaHhE
Havainnollistaa Notchproteiinin syntymisen ja funktion:
Notch https://www.youtube.com/watch?v=-BrI5qX9LBM
Wikipedia antaa seuraavaa englantilaista tekstiä, jota suomentelen, koska ei näy suomaalista versiota valmiina..
Notch signalointitie
Wikipediasta
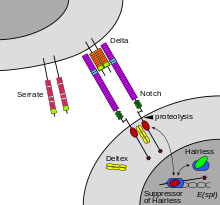
Notchvälitteinen juxtrakriininen signaali vierekkäisten solujen välissä
Notch signaloinnin vaiheet
Notch-signalointitie
on hyvin konservoitunut solusignalointijärjestelmä, jota esiintyy
useimmissa monisoluisissa organismeissa. Imettäväisissä on neljä
NOTCH-reseptoria ja niitä merkataan näin: NOTCH1, NOTCH2, NOTCH3 ja
NOTCH4.
Notchreseptori
on sellainen reseptoriproteiini, joka menee yhden kerran kalvon
läpi. Se on hetero-oligomeeri, jolla on iso solunulkoinen osa joka
liittyy kalsiumista riippuvalla tavalla ei-kovalenttisesti
notchproteiinin pienempään osaan. Tässä pienemmässä osassa on
lyhyt solun ulkopuolinen alue, yhden kerran kalvon läpi menevä
jakso ja pieni solun sisäinen alue.
Notchsignalointi
edistää neurogeneesin aikaista proliferoivaa signalointia ja Numb
estää sen aktiivisuutta edistämällä neuraalista erilasitumista
eli differentoitumista Notch omaa tärkeää osaa alkion
kehityksen säätelyssä.
Termejä:
notch receptors, NOTCH1, NOTCH2, NOTCH3, NOTCH4.
its activity is inhibited by Numb to promote neural differentiation.
Englantilainen sisällysluettelo artikkeliin: Contents
(1) Miten notch keksittiin?
Vuonna 1914 huomasi John S. Dexter banaanikärpsen siivissä kyhmyn. Geenialleellit tunnisti vuonna 1917 Thomas Hunt Morgan. Molekulaarinen analyysi ja sekvenssi havaittiin saman aikaisesti akhdella taholla 1980: Spyros Artavanis-Tsakonas ja Michael W. Young olivat nämä tiedemiehet. Kaksi C. elegansin Notch-geenialleellia tunnistettiin kehityksellisistä fenotyypeistä lin-12 ja glp-1. Samoihin aikoihin Iva Greenwald raportoi ” Drosophila Notch” lin-12 kloonauksen ja osittaisen sekvenssin.(2) Notchin toimintamekanismi
Notch -proteiini kulkee solukalvon läpi niin että osa sitä on solun sisällä, osa ulkona. Ligandiproteiinit sitoutuvat solunulkoiseen domeeniin ja saavat aikaan proteolyyttisen pilkkoutuman ja silloin vapautuu solun sisäinen domeeni ja menee solutumaan modifioimaan geenin ilmenemää.Pilkkoutumismalli ehdotettiin ensimmäistä kertaa vuonna 1993 ja se perustui niihin töihin, joita oli tehty Drosophila Notch ja C-elegans lin-12 geenistä. Tämä tutkimus antoi myös ensimmäistä tietoa onkogeenisestä mutaatiosta ihmisen Notch geenissä. Gary Struhl antoi vakuuttavan näytön tämän mallin puolesta vuonna 1998 analysoimalla Drosophilaa in vivo ja samoin Raphael Kopan soluviljelmillään. Alunperin mallia kyseenalaistettiin, mutta näytöt mallin puolesta todettiin kumoamattomiksi 2001.
Reseptori triggeröityy normaalisti suorasta solu-solukontaktista, jossa solujen transmembraaniset proteiinit muodostavat ligandeja suorassa kontaktissa ja sitoutuvat notch-reseptoriin. Notch-sitoutuminen sallii soluryhmien organisoitua keskenään siten , että yhden solun ilmentäessä tiettyä kantaa, naapurisolu voi kääntää sen vaihteen pois soluvälin notch-signaalilla. Täten soluryhmät vaikuttavat toinen toisiinsa tehden laajoja struktuureita. Tällä tavalla lateraalisen inhibition mekanismi on avain notch-signalointiin. Lin-12 ja Notch välittävät binaarisia solukohtalopäätöksiä ja lateraalinen inhibitio käsittää takaisinsyötön mekanismeja, mikä laajentaa alkuperäisiä eroavuuksia.
Notch-kaskadiin (tapahtumaketjuun) kuuluu Notch ja Notchin ligandit ja solunsisäiset proteiinit, jotka välittävät notch-signaalin solutumaan. Havaittiin, että Drosophila ja C. Elegans - eliöiden kehityksen aikaisessa solukohtaloiden erilaistumisessa oli osallistujana Notch/lin-12/Glp-1-reseptoriperhe. Notchin solun sisällä oleva domeeni tekee kompleksin CBF1:n ja Mastermindin (MAML1 ) kanssa aktivoiden kohdegeenien transkription kompleksin rakenne on määritelty.
Termejä:
CBF1 , Mastermind
CBF1= Recombining binding protein suppressor of hairless (RBPJ)
(3) Notchin funktiosta
Notch-signalointitie
on tärkeä solu-solukommunikaatiossa, joka käsittää
geenisäätelymekanismin kontrolloimassa moninaisia
solujen erilaistumisprosesseja alkiokehityksen ja aikuisuuden aikana.
Notch-signaloinnilla on osuutta myös seuraavissa prosesseissa.
- Neuronaalinen (hermo-) funktio ja kehitys
- Valtimosuonten sisäpinnan ( endoteelin) vakautumiskohtalot ja suonten uudismuodostus eli angiogeneesi
- Kriittisten solukommunikaatiotapahtumien säätely sydämen endokardiumin ja myokardiumin välillä sekä läppien varhaismuodostumisen että kammioiden kehittymisen ja erilaistumisen kuluessa.
- Sydänläppähomeostaasin muodostumisprosessissa; sovelluksia Notch- signaloinnin merkityksestä havaittavissa ihmisen kardiovaskulaarissa häiriöissä, muissakin kuin läppiä koskevissa. (Termi: cardiac valve homeostasis),
- Haiman exokriinisten ja endokriinisten solujen ajallinen erilaistuminen.
- Suoliston sekretoristen ja absorboivien solulinjojen muodostumisessa Notch-signalointi vaikuttaa solujen binaarisen kohtalon valintapäätöksiin.
- Luun kehityksessä hematopoieettisessa kantasoluaitiossa tapahtuva laajentuma erilaistumisessa: Päätetään osteoblastinen solulinja. Tämä viittaisi Notchin mahdolliseen terapeuttiseen osuuteen luun regeneroitumisessa ja osteoporoosissa.
- Laajentuma myös hemogeenisten endoteelisolujen alueella siinä signalointiakselissa, joka käsittää Hedgehog-signaloinnin ja Scl. (Termejä: Hedgehog signaling , Scl. https://en.wikipedia.org/wiki/Hedgehog_signaling_pathway)
- Päätökset lymfaattisen edeltäjäsolun johtamisista erilaisiin T-solulinjoihin.
- Rintarauhasen solulinjakohtaloiden päättämisen säätely useissa eri kehitysvaiheissa
- Mahdollisesti joitakin ei-nukleaaisia mekanismeja kuten aktiinistyoskeletonin kontrolli tyrosiinikinaasilla Abl. (Termi tyrosine kinase Abl ).
Notch-signalointi
on häiriytynyt monessa syövässä, ja virheellisestä
Notch-signaloinnnista on nähty viitteitä useissa taudeissa kuten
akuuttissa T-lymfoblastileukemiassa (T-ALL) sekä CADASIL-taudissa
(, joka on dominantisti autosomaalisti periytyvä aivovaltimotauti
jossa on aivokuoren alaisia infarkteja ja valkoisen aineksen
sairastumaa) , MS-taudissa, Fallotin tetralogiassa, Alagillen
oireyhtymässä ja monessa muussa tautitilassa.
Notch-signaloinnin
estämisestä on nähty anti-proliferatiivista vaikutusta akuutissa
T-lymfoblastileukemiassa soluviljelmissä ja eläinkoemalleissa. On
myös havaittu että Rex1 omaa estovaikutuksen mesenkymaalisten
kantasolujen Notch-ilmenemään estäen erilaistumsien. (Termi T-ALL , CADASIL, Multiple Sclerosis , Tetralogy of Fallot, Alagille syndrome, and many other disease Rex1).
O-linked glycans(4) Signalointitie
Notch-reseptorin
kypsymä käsittää sen tulevan solunulkoisen domeenin
pilkkoutumisen Golgin laitteen läpi tapahtuvan kulkeutumisen
aikana. Tuloksena on kaksiosainen proteiini, jossa on isompi
extrasellulaarinen domaani linkkiytyneenä pienempään
transmembraaniseen (plasmakalvossa olevaan) ja solunsisäiseen
domaaniin (NICD).
Toisesta
solusta tulevan ligandin (L) kiinnittyminen solun Notch-reseptoriin
edistää kahta proteiinia pilkkovaa prosessoitumistapahtumaa. Tämän
proteolyysin seurauksena solunsisäinen ( intrasellualarinen) domeeni
vaputuu (NICD) ja se voi mennä tumaan liittymään toisiin DNA:han
sitoutuviin proteiineihin (CSL, NICD, MAML,p300 kompleksina) ja täten säätelemään Notch-kohdegeenien expressiota.
Notch
samoinkuin useimmat sen ligandeista ovat transmembraanisia
proteiineja. Ligandia esittävän solun tullee (ehkä) olla Notchia
ilmentävän solun vierellä, jotta signalointia voi tapahtua.
Notch -ligandit ovat myös vain yhden kerran transmembraanisesti
kulkevia proteiineja ja ne ovat jäseniä DSL-perheessä (
Delta/serrate/LAG-2). Banaanikärpäsellä on kaksi ligandia, toinen
on Delta ja toinen Serrate nimeltään. Imettäväisissä vastaavat
nimet ovat Deltan kaltainen, Delta-like ja Jagged. Imettäväisissä
on multippeleita Delta-like ja Jagged-ligandeja ja amhdollisesti
valikoima muitakin ligandeja kuten F3/contactin.
Nematoda-lajissa
C.elegans kaksi geeniä koodaa homologisia proteiineja glp-1 ja
lin-12. Esiintyy ainakin yksi raportti, jonka mukaan olisi viitettä
siitäkin, että jotkut solut voisivat lähettää jatkeita, joiden
avulla signalointia tapahtuisi sellaistenkin solujen kesken, jotka
ovat 4-5 solun päässä toisistaan.
Notchin
extrasellulaarisessa domaanissa on pieniä cystiinipitoisia motiiveja
joita sanotaan EGF:n kaltaisiksi toistoiksi.
Esim.
Notch1 omaa 36 tällaista EGF-toistoa. Jokaisessa EGF:n kaltaisessa
toistossa on lähes 40 aminohappoa ja rakenne määräytyy pääosin
kuuden konsergoituneen cysteinitähteen perusteella ja ne muodostavat
kolme -S-S- (disulfidi) sidosta. Jokainen EGF-toistojakso voi
modifioitua O-linkkiytyneillä glykaaneilla spesifisissä kohdissa.
Yksi
O-glukoosisokeri voi asettua toisen ja kolmannen konservoituneen
cysteiinin väliin.
Ja
yksi O-fukoosi saattanee liittyä toisen ja kolmannen
konservoituneen cysteiinin väliin.
Näitä
sokereita lisää jokin toistaiseksi tuntematon
O-glykosyylitransferaasi (O-glukoosia)
ja
O- fukoosia vastaavasti GDP-fukoosiproteiini
O-fukosyylitransferaasi 1 (POFUT1).
O-fukoosin
lisääminen POFUT1- entsyymillä on absoluuttisesti välttämätöntä
Notch-funktiolle ja ilman tätä O-fukoosia lisäävää entsyymiä
ei mikään Notch-proteiini onnistu toimimaan kunnolla. Toistaiseksi
ei tiedetä täysin, millä tavalla Notchin glykosylaatio vaikuttaa
sen funktioon.
Notchin
O-glukoosi voi edelleen pidentyä (-O-Glc-Xyl-Xyl)
trisakkaridiksi
kahden xyloosisokerin lisällä, minkä tekee
xylosyylitransferaasit.
Notchin
O-fukoosi voi pidentyä tetrasakkaridiksi
(O-Fuc
-GlcNAc
-Gal-NeuAc)
entsyymien
yhteistyöllä:
N-Asetyyliglukosamini
-sokeria lisää GlcNAC-transferaasi nimeltään Fringe.
Galaktoosia
lisää gal-transferaasi .
Sialihappoa
(neuraminic acid)
lisää sialyltransferaasi.
Termejä:
O-glucose , O-glc
O-fucose , O-fuc
O-glucosyltransferase (except for Rumi)
GDP-fucose Protein O-fucosyltransferase 1 (POFUT1)
xylose , xyl
xylosyltransferases,
N-acetylglucosamine (GlcNAc)
N-Acetylglucosaminyltransferase , Fringe,
galactose . gal
galactosyltransferase,
sialic acid , neuraminic acid, NeuAc
sialyltransferase.
Lisää
monimutkaisuutta! Imettäväisillä on kolme Fringe
GlcNAc-transferaasia ja niillä on seuraavia nimiä ”lunatic
fringe” ”manic fringe” (raivoisat ainekset) ja ”radical
fringe” Nämä entsyymit vastaavat ns. fringe-vaikutuksesta
Notch-signalointiin. Fringe lisää GlcNAc O-fukoosisokeriin ja
sitten tapahtuu jatkossa galaktoosin ja sialihapon lisääminen. Kun
on läsnä tätä tetrasakkaridia, Notch signaloi vahvasti kun se
tekee vuorovaikutustaan Delta-ligandiin. mutta sen sijaan Notch-
siganlointi on huomattavan estynyttä Jagged- ligandin kanssa . Ei
ole aivan kirkasta käsitystä siitä, miten tämä sokerin
lisääminen inhiboi toisen ligandin kautta tapahtuvaa signalointia
ja vahvistaa taas toisen ligandin kautta tapahtuvan signaloinnin.
Kun Notchin extrasellulaarinen
domeeni (NECD)
on tehnyt interaktionsa toisen solun ligandin kanssa, eräs ADAM-
perheen metalloproteinaasi (ADAM10) pilkkoo Notch -proteiinin aivan
kalvon ulkopinnasta. Tämä vapauttaa Notchin extrasellulaarisen
pätkän (NECD), joka on edelleen interaktiossa ligandinsa kanssa.
Ligandi ja Notchin extrasellulaarinen pätkä (NECD) joutuvat
endosytoiduksi ligandin omaavaan soluun. Saattaa olla signaloivia
vaikutuksia ligandia ilmentävässä solussa tämän endosytoosin
jälkeen. Tämä osa Notchin funktiokartasta onkin intensiivisen
tutkimuksen alaa nykyään.
Tämän ensimmäisen
pilkkoutuman jälkeen gamma-sekretaasiksi kutsuttu entsyymi ( joka
tunnettaan AD-taudista) , pilkkoo jäljelle jääneen palan
Notch-proteiinista aivan plasmaklvon sisäpinnasta Notchia
ilmentävässä solussa.
Tällöin solunsisäinen
domaani (NICD) pääsee liikkumaan kohti tumaa, missä se voi
säädellä geeni-ilmenemää aktivoimalla transkriptiofaktorin
CSL. Alunperin luultiin, että nämä CSL-proteiinit vaimentaisivat
Notch- kohteen transkriptiota. Kuitenkin jatkotutkimuksissa kävi
ilmi, että NICD- pätkän, Notchin solunsisäisen domaanin
sitoutuminen kompleksiin saattaa sellaisen vaihteen päälle, että
CSL -repressorista tuleekin transkription aktivaattori. Notchin
solunsisäisen pätkän ( NICD) signalointikaskadiin osallistuu
muitakin proteiineja kuin CSL.
metalloprotease ( ADAM10)
γ-secretase
CSL.
(5) Ligandi- interaktio
Crystal structure of the Notch1-DLL4 complex depicted as the interaction is predicted to occur between two cells (PDB ID: 4XLW)
Kuvassa
näkyy punaisella Notch 1 reseptori ja vihreällä DLL4 ligandi.
Notch-signalointi
alkaa kun Notch-reseptori solun pinnalla liittyy lähellä olevan
solun ligandin kanssa vierekkäin ( trans-asemaan) . Vaikka Notchin
solunulkoinen (extrasellulaari) domaani on pitkä, niin kriittiset
määrääjät interaktiossa DLL4:n kanssa ovat kohdat EGF- 11 ja
-12. Alueet EGF-11 ja -12 ulkopinnassa ovat näitä ligandia
sitovia. EGF-8 domaani tunnistaa selektiivisesti Serrate/Jagged ja
EGF 6 - 15 domaanit vaaditaan maksimaaliseen signalointiin
ligandistimulaatiossa.
Notch1-Delta
like 4 – kompleksikiteen interkatioalueen tutkimuksissa nähtiin
milekyylitasoa ja selveni, että ligandin N-terminaalinen MNNL ( tai
C2) ja DSL-domaanit sitoutuvat Notchin domaaneihin EGF -12 ja -11
vastaavasti.
Notch1-Dll4-rakenne
myös valaisi Notchin O-linkkiytyneiden fukoosi- ja
glukoosi-yksiköiden suoraa osuutta ligandin tunnistamisessa ja
selvensi Notch- signaloinnin glykaanivälitteisen hienosäädön
rakenteellista mekanismia.
(6) Alkion aika, embryogeneesi
Notch-signalointitie
on tärkeä solu-solukommunikaatiossa ja säätelee alkion kehitystä.
Jatkotutkimukset nematodan C-elegans avulla viitaavat siihen,että
Notch-signalointi omaa huomattavaa osaa mesodermaalisessa induktiossa
ja solukohtaloitten määrämisessä.
ALKION
polaarisuus:
Notch-signalointia
tarvitaan polaarisuuden säätöön. Mutaatiotutkimuksissa on
havaittu, että Notch-signaloinnin puuttuminen kasvavista
somiiteista ( alkujaokkeista) aiheuttaa anterioris-posteriosista epänormaaliutta. (
anterior= etuosa , posterior on takaosa). Notch-signalointia
tarvitaan myös vasen-oikea asymmetrian määräytymiseen
selkärankaisilla
Termi:
somites, somiitit, alkujaokkeet
Somiitti, alkujaokke, Näitä muodostuu mesodemistä somitogeneesissä.
Somitogeneesissä
on Notch-signalointi keskeistä.Vuonna
1995 oli osoitettu hiirellä, että Notch1 oli tärkeä, jotta
somiitit olisivat koordinoidusti segmentoituneita.
Jatkotutkimuksissa tunnsitettiin notch1 rooliksi signalointi
segmentoitumisen kellossa, ajastuksessa. Näistä tutkimuksista
tehtiin oletus, että Notch-signaloinnin primäärinen funktio ei
oliskaan toimiminen yksittäisessä solussa, vaan soluajastuksen,
”solukellojen”, koordinoiminen ja niiden synkronisoituina
pitäminen. Tämä hypoteesi selitti Notch-signaloinnin
segmentoitumsien kehittymsiessä ja tätä tukee ne kokeet, joita on
tehty hiirillä ja zebrafish- kalalla, (eräällä karpin sukuisella
kalalla Danio rerio). Delta1mutantti hiirillä tehdyt kokeet
osoittiat epänormalin somitogeneesin josaa puuttui
anterior7posterior-polaarisuus ja tästä saatiin viitettä että
notxh-signalointi on valttämätön myös somiittien (
alkujaokkeitten) rajojen ylläpitämiseksi.
Termi:
somitogenesis. In somitogenesis, somites form from the paraxial (somitic) mesoderm,(7) Keskushermostojärjestelmän kehitys ja toiminta
Varhaislöydöt
Notch-signaloinnista keskushermostossa (CNS) saatiin banaanikärpsestä
mutageneesikokeista. Esim. havaittiin alkion letaali fenotyyppi
assosioituneena Notch-vikafunktioon ja se viittasi Notch - mutaation
voivan johtaa alkion varhaisvaiheessa neuraalisen ja epidermaalisen
solun eriämisen epäonnistumioseen banaanikärpäsalkiolla.
Viimeksi kuluneen vuosikymmenen aikana on tekniikka edistynyt
mutaatioitten ja poistogeenisyyden tutkimuksissa mikä sallii
Notch-siganlointitien tutkimisen myös nisäkäsmallissa kuten
jyrsijöissä.
Notch-signalointitie
havaittiin kriittiseksi pääasiassa neuraalisen progeniittorisolun
(NPC) ylläpidolle ja sen
itsestään
uudistumiselle. Viime vuosina on havaittu Notch-tielle
myös muita funktioita, kuten gliasolujen erilaistuminen,
neuronihermojen
kehitys
ja myös oppiminen ja muisti.
Neuronisolujen
erilaistuminen
Kehittyvässä
aivossa Notch-tie on välttämätön ylläpitämässä NPC-soluja ,
neuronin progeniittorisoluja. Tien aktivoituminen riittää
ylläpitämään NPC -soluja proliferoitumistilassa, kun taas
funktionkatoamismutaatiot Notch-signaalitien kriittisissä
komponenteissa aiheuttavat liian varhaisen neuronaalisen
erilaistumisen ja NPC- solujen vähenemisen. Notch-signaalin
modulaattorit esim Numb-proteiini, pystyvät vastavaikuttamaan
Notchin vaikutuksiin johtaen solusyklin pysähtymiseen ja
NPC-solujen differentioitumiseen. Tällä tavalla Notch -signalointi
kontrolloi NPC- solujen itsestään uudistumista ja solun
erilaistumiskohtaloita.
Notch-signaloinnin
ei-kanoninen haara, joka osallistuu STAT3 fosforylaatioon (Ser727)
ja sitä seuraavaan Hes3 expression lisääntyminen ,on näyttänyt
säätelevän lukuisia NPC soluja viljelmässä ja aikuisen
jyrsijän aivossa
Termi:
STAT3-Ser/Hes3
Signaling Axis, STAT3-Ser/Hes3
signaaliakseli
Aikuisessa
jyrsijässä ja soluviljelmässä Notch3 edistää neuronaalista
erilaisumista ja sillä on vastakkainen vaikutus kuin Notch1/2.
Tämä viittaa siihen, että yksittäiset Notch-reseptorit voivat
omata divergoivia funktioita riippuen soluyhteydestä.
Neuronin
kehityksestä
In
vitro- tutkimuksissa Notch voi vaikuttaa hermosolun kehittymiseen.
In vivo -tutkimuksissa Numb, Notch-signaloinnin modulaattori,
keskeyttää hermosolun kypsymisen kehittyvässä pikkuaivossa
(cerebellum), kun taas Numb-deleetio keskeyttää axonaalisen
arborisaation (haaroittumisen) sensorisessa gangliossa. Vaikka
tämän ilmiön taustamekanismi ei ole selvä, löydöt yhdessä
viittaavat siihen, että Notch-signalointi on kriittinen neuronin
kypsymiselle.
Glia-solujen
kehityksestä
Notch
näyttää omaavan gliogeneesissä ohjaavaa osaa ja saattaa suoraan
edistää monen gliasolualatyypin erilaistumsita. Esimerkiksi
Notch-signaloinnin aktivoiminen verkkokalvossa suosii Müllerin
gliasolujen kehkeytymisiä neuronien kustannuksella, kun taas
vähentynyt Notch-signalointi indusoi gangliosolujen tuotantoa
aiheuttaen vähenemää Müllerin gliasolujen lukumäärässä.
Termejä:
gliogenesis,glial cell subtypes.
Muller glia cells
Aikuisen
aivofunktio
Kehityksellisten
funktioittensa lisäksi Notch-proteiineilla ja ligandeilla on
ilmenemänsä aikuisen hermojärejstelmän soluissa, mikä viittaa
osuuteen koko elämänaikaisessa keskushermostojärjestelmän
plastisuudessa. Jos aikuishiirillä on mutaatioita joko Notch1:ssä
tai Cbf1:ssä sillä näuyttää olevan puutteita spatiaalisessa (
paikkaan ja tilavuuteen liittyvässä) oppimisessa ja muistissa.
Samanlaisia tuloksia on saatu tutkittaessa Notch-proteiinin
kalvonsisäistä ( intramembraanista) pilkkoutumista välittäviä
preseniliini-1ja -2- proteiineja. Täsmentäen: preseniliinien
ehdollinen deleetio excitatorisissa neuroneissa 3 viikkoa hiiren
syntymästä aiheuttaa aikuishiirille oppimisen ja muistin vajeita,
hermojen vikafunktiota ja asteittaista neurodegeneraatiota. Monet
gammasekretaasin estäjät joita käytettiin AD-taudin MCI:n
kliinisiin kokeisiin asti johtivat statistisesti kognition
huononemaan kontrolleihin verrattuna , minkä katsottiin johtuvan
insidentaalisesta vaikutuksesta Notch -signalointiin
Termejä:
presenilins1
and 2,
gamma secretase inhibitors
MCI
(8) Sydämen ja verisuonten kehitys
Kardiovaskulaarinen
( sydämen ja verisuoniston) kehitys
Notch-signalointitie
on kriittinen komponentti sydämen ja verisuoniston muodostumisessa
ja morfogeneesissä sekä kehityksen aikana että taudeissa. Se
vaaditaan endoteelisten kärki- ja varsisolujen valintaan
angiogeneettisen haaroittumisen aikana.
Termi:
Sydämen kehittyminen
Notch-signaalitiellä
on kriittinen osuus ainakin kolmessa sydämen kehityksellisessä
prosessissa. Eteiskammiokanavan kehittymisessä, sydänlihaksen
kehittymisessä ja sydämestä poisjohtavan vuoalueen
kehittymisessä
Termejä:
Eteiskammiokanavan
kehittyminen
-
Eteiskammiorajan muodostuminen
Notch-signalointi
voi säätää eteiskammiorajan muodostumista eteiskammiokanavan ja
sydänlihaskammion välille.Tutkimuksista on selvinnyt, että Notch
tien puuttumisesta tai ylisäädöstä voi seurata
eteiskammiokanavan kehityksellisiä puutoksia. Lisäksi Notchin
kohdegeenit HEY1 ja HEY2 osallistuvat kahden kriittisen
säätelyproteiinin ilmenemän rajoittamiseen eteiskammiokanavaan ja
nämä säätelyproteiinit ovat BMP2 ja Tbx2
Termejä: the Notch target genes HEY1 and HEY2
-
Eteiskammioalueen epiteeliaalismesenkymaalinen transitio (EMT)
Notch-signalointi
on myös tärkeä tässä atriovenrikulaarisessa transitiossa
epiteliaalisesta mesenkymaaliseksi (EMT)
, mikä vaaditaan
atriovenrikulaarisen kanavan kypsymiseen. Sen jälkeen kun
eteiskammioraja on muodostunut,
alaryhmä atrioventrikulaarista kanavaa verhoavista
endokardiaalisista
soluista aktivoituu myokardiumista lähtevistä signaaleista, ja
inter-endokardiaalisilla
signalointiteillä tapahtuu muuntuminen epiteliaalisesta
mesenkymaaliseksi (EMT).
Notch1-vaje johtaa
puuteelliseen EMT-induktioon: Hyvin harva migroituva solu on
havaittavissa ja niistä puuttuu mesenkymaalinen morfologia.
Notch
saattaa säätää tätä EMT-
prosessia aktivoimalla
matrixmetalloproteaasi 2.n (MMP2) ilmenemän. Tai estämällä
vaskulaarisen endoteliaalisen kadheriinin ilmenemän
AV-kanavan endokardiumissa
ja suppressoimalla
VEGF-tien , joka käyttää VEGFR2.
RBPJk/CBF1- kohdennetuissa
mutanteissa sydämen läppien kehitys on vahvasti häiriintynyt
oletettavasti koska endokardiumin kypsyminen ja signalointi ovat
viallisia.
Termejä:
EMT,
matrix metalloproteinase2 (MMP2)
Kammioiden
kehittyminen
Eräät
tutkimukset Xenopuksella ja hiiren alkion kantasoluilla viittaavat
siihen, että kadiomyogeeninen määräytyminen ja erilaistuminen
vaativat Notch-signaloinnin inhibition.
Aktiivinen Notch-signalointi
vaaditaan sydänkammion endokardiumissa asianmukaisen
trabekulaation kehittymiseen myokardiaalisen erikoistumisen
jälkeen BMP10, NRG1 ja EphrinB2 ilmenemän säädöllä.
Notch-signaloinnin
alavirran vaikuttaja, HEY2 on myös osoitettu tärkeäksi kammion
kehityksen säätelyssä ja sitä ilmenee kammioiden väliseinämässä
septumissa ja sydäntyynyjen endocardiaalisissa soluissa.
Kardiomyosyytti - ja sileä lihassoluspesifinen HEY2-deleetio johtaa
huonontuneeseen sydämen supistuskykyyn, epämuotoiseen oikeaan
eteiseen ja kammioiden välisen septumin puutoksiin.
Termejä:
Xenopus endocardium
BMP10,
NRG1,
EphrinB2
septum
cardiac cushions
Kammion
ulosvirtausalueen kehitys
Aortankaaren ja aortankaaren
valtimoitten kehityksen aikana on Notch-reseptoreilla, ligandeilla ja
kohdegeeneilla ainutlaatuinen ilmenemismallinsa. Jos Notch-tie oli
blokeerattuna, epäonnistui verisuoniston silean lihassolun
merkitsijän ilmeneminen, mikä viittaa siihen, että Notch on
osallisena kardiaalisen neuraalipoimun solujen erilaistumisessa
verisuonistosoluiksi ulosvirtausalueen kehityksen aikana.
Termi:
vascular smooth muscle cell marker Angiogenesis
Endoteliaaliset
solut käyttävät Notch-signalointitietä koordinoidessaan solujen
käyttäytymisiä verisuonten haaroittumisen (ja versoilun) aikana,
mitä angiogeneesissä tapahtuu. Notchin aktivaatio primääristi
tapahtuu suorassa interaktiossa Notch-ligandiin DLL4
”konnektorisolussa” ( jotka ovat liittynyt ) ja soluissa
,jotka verhoavat tiivistä stabiilia verisuonta. Deltan kaltaista
ligandia 4 (DLL4) ilmenee endoteliaalisissa kärkisoluissa.
VEGF-signalointi
on tärkeä tekijä endoteelisolujen migraatiolle ja
proliferaatiolle ja se saattaa olla alas säätyneenä soluissa,
joissa Notch-signalointi on aktiivina ja alentanut Vegf-reseptorin
transkription pitoisuudet. Zebrafish- kalan tutkimuksista on saatu
tietää, että kala-alkiolla, jolta puuttuu Notch -signalointi,
ilmenee ektooppista ja pinttynyttä VEGF3:n zebrafish-ortologia,
flt4 kaikissa endoteliaalisissa soluissa , kun taas Notch-aktivaatio
vaimentaa täydellisesti sen ilmenemän.
Saattaa
olla, että Notch-signalointi kontrolloi verisuonten versomismallia
angiogeneesin aikana. Kun solut ehjässä suonessa altistetaan
VEGF-signaloinnille, vain rajoittunut määrä suonista aloittaa
angiogeenisen prosessiin (uuden haarqan tekemisen). Vegf kykenee
indusoimaan DLL4-excpressiota. Vuorostaan DLL4-ää ilmentävät
solut säätävät alas Vegf-reseptoria lähisoluissa aktivoimalla
Notchin ja siten estämällä solujen migraatiota kehittyvään
versoon ( haaraan). Samoin varsinaisen haaroittumisprosessin aikana
konnektorisolujen migratorisen käyttäytymisen täytyy olla
rajoittunutta, jota ehjä yhteys alkuperäiseen verisuoneen
saadaan pysytettyä.
Termejä
Endothelial angiogenesis.Delta-like ligand 4 (Dll4)
VEGF
DLL4
9. Sisäeritysjärjestelmän kehitys
Haiman kehityksestä
Varhaiskehityksen
aikana alkaa haiman ( pancreas) muodostuminen endodermistä.
Notch-signalointitien elementtejä on havaittu kehittyvässä
haimassa, mikä viittaa siihen, että Notch-signalointi on tärkeä
haiman kehityksessä. On näyttöä siitä, että Notch -signalointi
säätelee endokriinisten solutyyppien progressiivista
rekrytoimista yleisestä esisolusta ja tätä Notch vaikuttaa
kahta tietä.
Toinen
tie on ”lateraalisen inhibition” tie, joka tarkentaa jotkut solut
primääreiksi ja jotkut solut sekundaareiksi niissä soluissa,
joilla on potentiaalia samaan kohtaloon päätymiseen. Lateraali
inhibitio vaaditaan monen solutyypin jatkolinjan määräytymiseen.
Tässä voisi löytyä selitystä siihen, miksi endokriinisest solut
sijaitsevat hajallaan pankreasepiteelissä.
Toinen
mekanismi puolestaan on ” suppressiivinen ylläpito”, mikä
selittäisi Notch-signaloinnin osuuden haiman erilaistumisessa.
Tässä aktiviteetissä arvellaan fibroblastikasvutekijällä 10
(FGF10) olevan tärkeää osuutta, mutta yksityiskohdat ovat
epäselviä.
Suoliston
kehityksestä
Notch-signaloinnin
merkityksestä suolen kehityksen säätelyssä on saatu viitettä
useista raporteista. Notch-signalointitien elementtien mutaatiot
vaikuttavat varhaisimpien suolistosoolujen kohtalon päätymiin
zebrafish- kalan kehittymisestä saadun tiedon mukaan.
Transkriptioanalyysit ja funktionaaliset tutkimukset paljastavat,
että Notch-signalointi kohdistuu suolessa Hes1-tekijään ja
säätelee binaarisen solun joutumista joko absorptiivisen tai
sekretorisen solun linjalle.
Luun
kehitys
Varhaisissa
in vitro-tutkimuksissa havaittiin Notch-signalointitietä
osteoklastogeneesin vaimennussäädössä ja osteoblastogeneesissa.
Notch1 ilmeni mesenkymaalisessa tihentymässä ja siitä seuraten
hypertrofisissa kondrosyyteissä ruston muodostuksessa
(chondrogenesis) . Notch- signaloinnin yliesiintymä esti BMP2:n
indusoimaa osteoblastin differentoitumista. Kaiken kaikkiaan
Notch-signaloinnilla on suuri osuus mesenkymaalisen solun
päätymisestä osteoblastilinjalle ja tästä voidaan löytää
terapeuttisia lähestymistapoja luun regeneraatioon.
Termejä::
osteoclastogenesis osteoblastogenesis.
chondrocytes
10. Respiratorisen systeemin kehitys
Notch ei osallistu kehkoalveolien kehittymiseen.termejä: alveoli , lung.
11. Syöpä
Koska Notch- signalointi osallistuu moniin syöpiin, on alettu tutkia Notchin estäjiä (erityisesti gammasekretaasin estäjiä) syövän hoitoon. Vuonna 2013 oli 7 Notch-inhibiittoria kliinisissä kokeissa. MK-0752- nimisestä on saatu lupaavia tuloksia rintasyövän varhaisista kliinisistä kokeista Termejä: notch inhibitors , gamma-secretase inhibitors)
12. LinkkejäDiagram: Notch signaling in Drosophila
Netpath - A curated resource of signal transduction pathways in humans
Notch Receptors at the US National Library of Medicine Medical Subject Headings (MeSH)
13. References: Kts. Wikilähde.
Muistiin 30.11. 2016


Inga kommentarer:
Skicka en kommentar